NADPH Oxydase
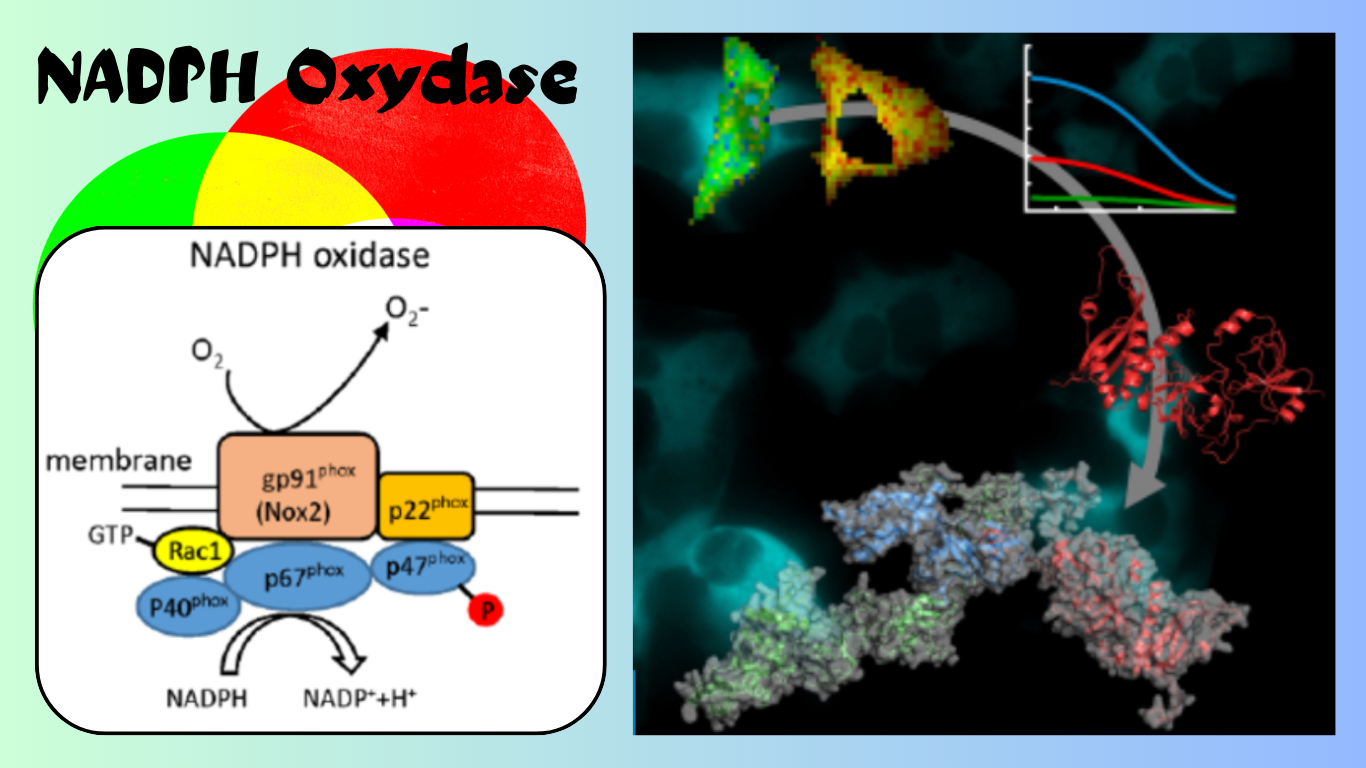
Les Nox sont des hémoprotéines transmembranaires et des transporteurs d’électrons, sont les seules enzymes connues dont la génération d’espèces réactives de l’oxygène (ROS). Souvent décrites comme les producteurs de ROS, leurs fonction et de catalyser la réduction l’oxygène moléculaire en anion superoxyde (O2*-) pour donner des ROS. Ces oxydants sont produites en excès dans les maladies chroniques et les pathologies liés au vieillissement.
Les espèces réactives de l’oxygène (ROS), le superoxyde (O2*-) et le peroxyde d’hydrogène (H2O2) jouent un rôle important dans la signalisation cellulaire et le système immunitaire, et sont générés par des enzymes appartenant à la famille des Nicotinamide Adénine Dinucléotide Phosphate (NADPH) oxydase (NOX).
Chez l’homme, la famille NOX se compose de sept membres qui diffèrent par la production de ROS, la composition des sous-unités, le mécanisme de régulation et la distribution tissulaire. La NOX-2 est la plus étudié est exprimé principalement dans les cellules phagocytaires telles que les neutrophiles et les macrophages, elle est responsable de la production de superoxyde pendant la poussée respiratoire, cad, L’explosion oxydative, ou explosion respiratoire (respiratory burst en anglais), est la libération rapide de dérivés réactifs de l’oxygène, où les ROS sont rapidement générés dans les phagosomes pour détruire les agents pathogènes microbiens.
NADPH oxydase réduis le dioxygène (O2) en ion superoxyde (O2*-) qui sera converti en peroxyde d’hydrogène (H2O2). Une autre enzyme, la myéloperoxydase (MPO), convertit H2O2 en HOCl. Le superoxyde O2*-, le peroxyde d’hydrogène H2O2 et l’acide hypochloreux HOCl constituent les espèces réactives de l’oxygène détruisant les agents pathogène par oxydation.
Étude expérimentale de Fenton
Avec Réactif de Fenton, Le mélange du fer ferreux et le peroxyde d’hydrogène constitue un très bon oxydant pour de nombreux composés organiques. Au cours de la réaction, le peroxyde d’hydrogène (H2O2) oxyde le fer ferreux (Fe2+) oxydé en fer ferrique (Fe3+), produisant un ion hydroxyde OH- et un radical libre hydroxyle *OH, selon la réaction d’oxydoréduction, le bilan est le suivant : H2O2 + Fe2+ — Fe3 + OH- + *OH. Il paraît que cette particule Hydroxylé (*OH) est classée parmi les radicaux libres-ROS-les plus oxydants.